
Źródła związków azotowych w nowych zbiornikach.
Pierwsze dni funkcjonowania zbiornika to trudny okres dla akwarysty. Dopiero co urządzone akwarium początkowo sprawia radość i jest powodem do dumy, jednak po kilku dniach często okazuję się czarnym snem, kiedy w zbiorniku pojawiają się nieproszeni goście – algi. Główna przyczyną problemów jest brak lub zbyt małe kolonie pożytecznych bakterii. Nagromadzenie związków azotowych (głównie amonowych), węgiel organiczny, fosforany w połączeniu z silnym oświetleniem są doskonałą pożywką wszelkiego rodzaju glonów pierwotniaków i okrzemek (jeśli w wodzie występują również krzemiany). Źródłami azotu w świeżo założonym akwarium mogą być miedzy podłoża np. ziemia ogrodowa, substraty lub tzw. „soile” typu japońskiego, rośliny (np.: degradujące się liście, łodygi), resztki pożywki in vitro oraz korzenie użyte do aranżacji. W podłożach najczęściej azot występuje w postaci amonowej NH4+, azotanowej NO3– w niewielkich ilościach mogą występować azotyny NO2– , mocznik lub jego pochodne. Uszkodzone lub degradujące się rośliny, wydzielają do wody białka i aminokwasy, które w wyniku amonifikacji konwertowane są głównie do jonów amonowych[1].
Znaczenie tlenu w procesach nitryfikacji
Nitryfikacja to proces dwuetapowy w można go przedstawić za pomocą uproszczonych reakcji[2]:
Etap I : NH4+ + 2O2 →NO2– + 2H2O
Etap II : NO2– + 1/2O2 → NO3–
W każdym w dwóch etapów niezbędnym substratem jest tlen. Wniosek z tego, że bakterie nitryfikacyjne to bakterie aerobowe (tlenowe), które wymagają do prawidłowego metabolizmu niezakłóconego dostępu do tlenu. Zapotrzebowanie na tlen w nitryfikacji jest bardzo duże, aby utlenić 1g azotu amonowego do azotanów musimy dostarczyć około 4,5g tlenu. Należy pamiętać, że jest to tylko jeden z wielu procesów zużywających tlen w naszym akwarium, dlatego powinniśmy zadbać o dobre napowietrzanie zbiornika szczególne, gdy oświetlenie nie pracuje (rośliny nie fotosyntezują)[3]. Stechiometryczne potrzeba 4 razy więcej tlenu do reakcji w etapie I niż w etapie II. Jednak o ile w wodzie do reakcji etapu I wystarcza stężenie O2 na poziomie 2mg/l, to aby zaszła reakcja etapu II stężenie tlenu musi być około dwukrotnie wyższe[4]. Szybkość nitryfikacji względem stężenia rozpuszczonego tlenu w wodzie przedstawia wykres[5,6]:
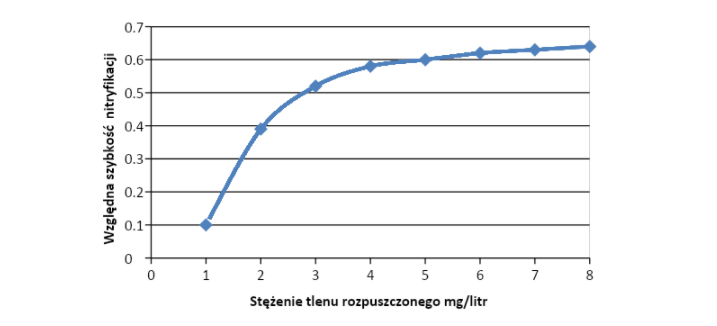
Jeżeli stężenie tlenu nie jest wystarczająco wysokie wówczas zachodzi denitryfikacja oraz oddychanie azotanowe, prowadzące do powstawania azotynów(NO2–) z jonów azotanowych(NO3–)[7]. Wykres zależności szybkości względnej denitryfikacji od stężenia tlenu rozpuszczonego ilustruje wykres[6]:
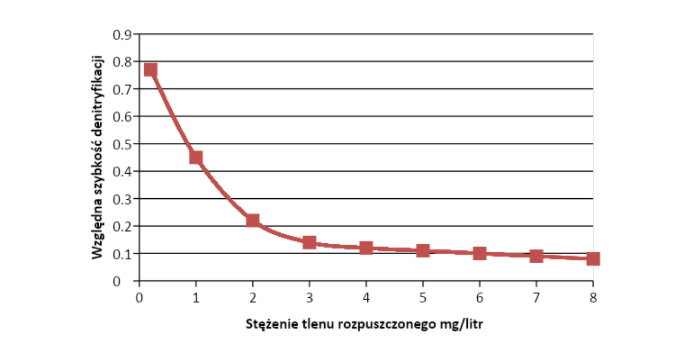
Ogólnie rzecz biorąc denitryfikacja jest zjawiskiem korzystnym powodującym samooczyszczanie się zbiorników wodnych. Odmienna sytuacja występuje w akwariach roślinnych, gdzie konsumpcja azotu jest relatywnie wysoka. Zjawisko denitryfikacji jest niekorzystne ponieważ powoduje straty azotu i przyczynić się zaburzenia współczynnika Redfielda[1].
[1] Badania własne 2016-2019.
[2] Gerhard Richter „Procesy metaboliczne u roślin” PWN 1975.
[3] Zurzycki J. Michniewicz M. „Fizjologia roślin” PWRiL 1979.
[4] dr inż. Joanna Jeż – Walkowiak, mgr inż. Łukasz Weber „Usuwanie jonu amonowego z wody podziemnej”, 2008.
[5] Michael K.Stenstrom, Richard A.Poduska, „The effect of dissolved oxygen concentration on nitrification” Water Research Vol. 16 page 643-649. 1980.
[6] Sharil Niza B Abdul Aziz „Effect of dissolved oxygen concentration on nitrification and denitryfikation” 2005.
[7] Diana Walstad „Rośliny w akwarium. Ekologia roślin wodnych” Oriol 2007.